Indicador de logro: Reconoce e interpreta el origen de la tabla periódica.
Competencia: Reconozco e interpreto el origen de la tabla periódica.
Palabras claves: Elementos químicos, científicos, peso atómico, grupo, período, Mendeleiev, tabla periódica.
Pregunta generadora:
¿Por qué es importante reconocer e interpretar el origen de la tabla periódica?
Situación de aprendizaje:
Para los primeros hombres , la materia estaba compuesta por agua, tierra, aire y fuego. Hoy en día se conocen más de un centenar de elementos.
Origen de la tabla periódica
Vídeo motivacional: https://www.youtube.com/watch?v=YJ-XDj_KrHY
En la medida que fue aumentando el número de elementos surgió la necesidad de clasificarlos; Johann Dobereiner en 1817 lo hizó por el peso atómico igual y los denomino triadas, en las que aparecía la misma relación.
Posteriormente John Nelands en 1864, ordeno los elementos observando que, el octavo elemento a partir de uno cualquiera, tenia las mismas propiedades químicas del primero. Así por ejemplo, quedaron en el mismo grupo el litio, el sodio y el potasio, etc. Sin embargo más allá de algunos elementos, las octavas ya no podían aplicarse.
Para 1871 Dimitri Mendeleiev ruso y Lothar Meyer alemán, independientemente propusieron una nueva clasificación de los 61 elementos conocidos hasta ese entonces. Mendeleiev organizó los elementos según su orden creciente de pesos atómicos, y los agrupo en líneas horizontales o períodos y en columnas verticales o grupos, todos los elementos de un mismo grupo presentaban propiedades químicas semejantes. Mendeleiev estableció la ley periódica, que dice que las propiedades de los elementos químicos no son arbitrarias, sino que dependen de la estructura del átomo y varían de una manera periódica con respecto al peso atómico.
Para la época moderna el físico inglés Henry Moseley en 1914 manifestó que las propiedades de los elementos dependen más de sus números atómicos que de sus pesos atómicos, así se corregía algunas irregularidades con el potasio, argón, níquel, cobalto yodo y telurio, modificando la anterior tabla de Mendeleiev, Según la nueva ley, las propiedades físicas y químicas de los elementos varían en forma periódica con respecto a sus números atómicos.
La estructura de la tabla periódica moderna se organiza en grupos y períodos.
Los grupos corresponden a las columnas verticales y dichos elementos presentan propiedades similares. Tienen el mismo número de electrones en su última capa o últimas capas.
Organización de la tabla periódica
El período corresponde a las filas horizontales y un elemento coincide con su última capa electrónica; es decir un elemento con cinco capas electrónicas estará en el quinto período. Por ejemplo el hierro Fe pertenece al cuarto período, ya que tiene cuatro capas electrónicas.
Vídeo de apoyo: https://www.youtube.com/watch?v=65dDwvVHAv0&index=13&list=PL373A21734DDE957E
Regiones de la tabla periódica. Se presenta por la ubicación de los elementos y el subnivel al que pertenecen los electrones de su último nivel. En la taba periódica encontramos cuatro regiones: s, p, d y f
Regiones de la tabla periódica
Para ubicar un elemento en la tabla siga las siguientes indicaciones: https://www.youtube.com/watch?v=8mI0sYypdLQ
Clasificación y propiedades de los elementos
Actividad motivacional:
Cuento "La fiesta Periódica": http://studylib.es/doc/776863/la-fiesta-peri%C3%B3dica-autora--anna-kalkanis-en-un-lugar-muy
Los elementos de la tabla periódica se clasifican en metales y no metales y en algunas ocasiones se habla de un tercer grupo denominado metaloides.
Los metales poseen brillo, conducen el calor y la electricidad, son dúctiles y maleables. por lo general a temperatura ambiente son sólidos a excepción del mercurio. Cuando se combinan químicamente tienen tendencia a donar electrones.
Los no metales poseen propiedades contrarias a los metales. No tienen brillo, no conducen el calor ni la electricidad. se usan como aislantes, no son dúctiles ni maleables y en general se encuentran en los tres estados.
Los metaloides son elementos que tienen propiedades intermedias entre los metales y no metales. En la tabla se ubican entre los metales y no metales.
Grupos de la tabla periódica
Un grupo es una columna de la tabla. Hay 18 grupos en la tabla periódica. Muchos de estos elementos químicos corresponden a familias conocidas, se ideó para ordenar estas familias de una forma coherente y fácil de ver. Los elementos de un grupo tienen configuraciones electrónicas similares en los niveles de energía más exteriores, así los elementos de un mismo grupo tienen propiedades físicas y químicas muy semejantes.
En la actualidad los grupos se enumeran utilizando los números arábigos; la primera columna es el grupo 1, la segunda el grupo 2, y así hasta la decimoctava que corresponde al grupo 18.
Al grupo 1 pertenecen los metales alcalinos.
Al grupo 2 pertenecen los metales alcalinotérreos
Del grupo 3 al 12 pertenecen los metales de transición o elementos del bloque F, denominados lantánidos y actínidos.
Al grupo 13 pertenecen los térreos.
Al grupo 14 pertenecen los carbonoides.
Al grupo 15 pertenecen los nitrogenoides.
Al grupo 16 pertenecen los anfígenos o calcógenos.
Al grupo 17 pertenecen los halógenos.
Al grupo 18 pertenecen los gases nobles.
Así, por ejemplo, si observamos la configuración electrónica de los elementos del PRIMER GRUPO, el grupo 1 o alcalinos
Elemento
|
Símbolo
|
Última capa
|
Hidrógeno
|
H
|
1s1
|
Litio
|
Li
|
2s1
|
Sodio
|
Na
|
3s1
|
Potasio
|
K
|
4s1
|
Rubidio
|
Rb
|
5s1
|
Cesio
|
Cs
|
6s1
|
francio
|
Fr
|
7s1
|
La configuración electrónica de su última capa es igual, variando únicamente el periodo del elemento
Períodos de la tabla
Un periodo es una fila horizontal de la tabla. El número de niveles energéticos de un átomo determina el periodo al que pertenece. Cada nivel está dividido en distintos subniveles, y así aumenta su número atómico. los elementos en el mismo periodo tienen características similares en radio atómico, energía de ionización, afinidad electrónica y electronegatividad.
la tabla periódica tiene siete periodos, identificados con las letras: K, L, M, N, O, P, Q o con los números arábigos 1, 2, 3, 4, 5, 6, 7.
Los períodos no son todos iguales, sino que el número de elementos que contiene va cambiando, aumentando al bajar en la tabla periódica.
Así, el primer período tiene sólo dos elementos: el Hidrógeno y el Helio.
Período 1 (2 elementos)
|
El segundo y tercer períodos tienen ocho elementos.
Período 3 (8 elementos)
El cuarto y quinto períodos tienen dieciocho elementos.
Período 4(18 elementos)
El sexto período tiene treinta y dos elementos.
Período 6 (32 elementos)
El séptimo período no tiene los treinta y dos elementos.
Nota: El período que ocupa un elemento coincide con su última capa electrónica. Es decir, un elemento con cinco capas electrónicas , estará en el quinto período y así sucesivamente.
Regiones o bloques de la tabla periódica
La tabla periódica se puede también dividir en regiones o bloques de elementos según el orbital que estén ocupando los electrones más externos.
Regiones o bloques según el orbital
Las regiones o bloques han sido denominados por las letras s, p, d y f.
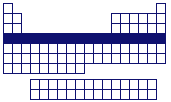
Los elementos de la región s son aquellos situados en los grupos 1 y 2 de la tabla periódica. En estos elementos el nivel energético más externo corresponde a orbitales s.
Elementos de la región S
Z
|
Nombre
|
Símbolo
|
1
|
Hidrógeno
|
H
|
2
|
Helio
|
He
|
3
|
Litio
|
Li
|
4
|
Berilio
|
Be
|
11
|
Sodio
|
Na
|
12
|
Magnesio
|
Mg
|
19
|
Potasio
|
K
|
20
|
Calcio
|
Ca
|
37
|
Rubidio
|
Rb
|
38
|
Estroncio
|
Sr
|
55
|
Cesio
|
Cs
|
56
|
Bario
|
Ba
|
87
|
Francio
|
Fr
|
88
|
Radio
|
Ra
|
Los elementos de la región p son aquellos situados en los grupos 13 al 18. En estos elementos el nivel energético más externo corresponde a orbitales p.
Los elementos de la región d son aquellos situados en los grupos 3 a 12 de la tabla periódica. En estos elementos el nivel energético más externo corresponde a orbitales d.
Los elementos de la región f, son los elementos de transición; son dos series, una comenzando por el elemento Lantano y la otra a partir del Actinio, llamados en su orden Lantánidos y actínidos.
El número atómico
El número atómico es la identidad de un átomo y sus propiedades que vienen dadas por el número de partículas que contiene. Un elemento se diferencia de otros por el número de protones que tienen sus átomos en el núcleo; y se representa con la letra Z. Por ejemplo: El Litio tiene 3 protones y su Z es igual a 3: (Z=3). El Hidrógeno tiene un protón y su Z es igual a 1: (Z=1).
Características que presenta
un átomo de Hidrógeno
El número atómico permitió clasificar a los elementos en la tabla periódica en un orden creciente: 1, 2, 3, 4....118.
La masa atómica
Es la cantidad de materia que tiene un átomo, se identifica con la letra A y se obtiene de sumar el número protones más el número de neutrones
( Z+N=A ).
Aunque todos los átomos de un mismo elemento se caracterizan por tener el mismo número atómico, pueden tener distinto número de neutrones. Llamamos isótopos a las formas atómicas de un mismo elemento que se diferencian en su masa atómica.
Una forma de conocer el número de neutrones es restando de la masa atómica el número de protones; así, por ejemplo:
La masa atómica del hierro es 55,847 la aproximamos a 56. El Z del hierro es 26; entonces a 56 le restamos 26 siendo igual a 30; luego el número de neutrones en el átomo de hierro es 30.
Para entretenerse un ratito:
http://www3.gobiernodecanarias.org/medusa/lentiscal/1-CDQuimica-TIC/applets/tablaperiodicamuda/jtpmuda.htm
* Santillana 7 ISBN958-24-1081-7
+http://recursostic.educacion.es/secundaria/edad/4esofisicaquimica/4quincena8/4q8_contenidos_3c_ampliacion.htm
* YUOTUBE https://www.youtube.com/watch?v=65dDwvVHAv0
*http://www.virtual.unal.edu.co/cursos/ciencias/mtria_ensenanza/tabla_periodica/flash/4_01.swf
* http://studylib.es/doc/261415/una-fiesta-muy-elemental-file
+https://www.youtube.com/watch?v=O8uXEhdSwOA
+ https://www.youtube.com/watch?v=3I3hoC4lOPM&nohtml5=False